1 / 2015 / vol. 4
Kosmetologia Estetyczna
105
artykuł naukowy
Kosmetologia Estetyczna
N
Za sukces uważane jest uzyskanie nawet niewielkiej
rozpuszczalności ftalocyjanin. Wiele rozpuszczalnych
w wodzie porfiryn, zarówno z grupy anionowych, jak
i kationowych tworzy agregaty z albuminami, główny-
mi składnikami osocza krwi, co jest krytycznie ważne
w PDT [4].
Agregaty, zawierające kompleks porfiryny z białkiem,
mogą łatwiej pokonywać błonę komórkową, co w rezul-
tacie podnosi ich efektywnośćw terapii. Makrocząsteczki
poprawiają skuteczność biodystrybucji kompleksów por-
firyn z metalami, zaś badanie połączeń porfiryn z białka-
mi pozwala na lepsze zrozumienie mechanizmu lokalizo-
wania fotosensybilizatoróww guzach nowotworowych.
Woparciu o powyższe i bazując na dotychczasowych
doniesieniach naukowych, pojawiła się idea ich wy-
korzystania w diagnostyce i terapii fotodynamicznej.
Światło z zakresu bliskiej podczerwieni może przeni-
kać w tkanki na dość dużą głębokość, do kilku centyme-
trów. Z tego względu, wykorzystanie kompleksów por-
firyn i ftalocyjanin cyrkonu i wybranych lantanowców
jest jak najbardziej uzasadnione. Prace, poświęcone za-
stosowaniu kompleksów lantanowców jako czynników
fotosensibilizacyjnych w terapii fotodynamicznej oraz
markerów komórek nowotworowych, stwarzają duże
możliwości połączenia właściwości, które mają porfiry-
ny i ftalocyjaniny z właściwościami lantanowce [5-7].
Przeprowadzone wcześniej badania nad kompleksami
aksjalnie podstawionych monoftalocyjanin lantanow-
ców w żelach krzemionkowych wskazują na obecność
efektywnego transferu elektronów pomiędzy ligan-
dem a jonem lantanowca, co z kolei jest warunkiem
koniecznym do wytworzenia singletowego tlenu lub
możliwości tworzenia wolnych rodników [8-10].
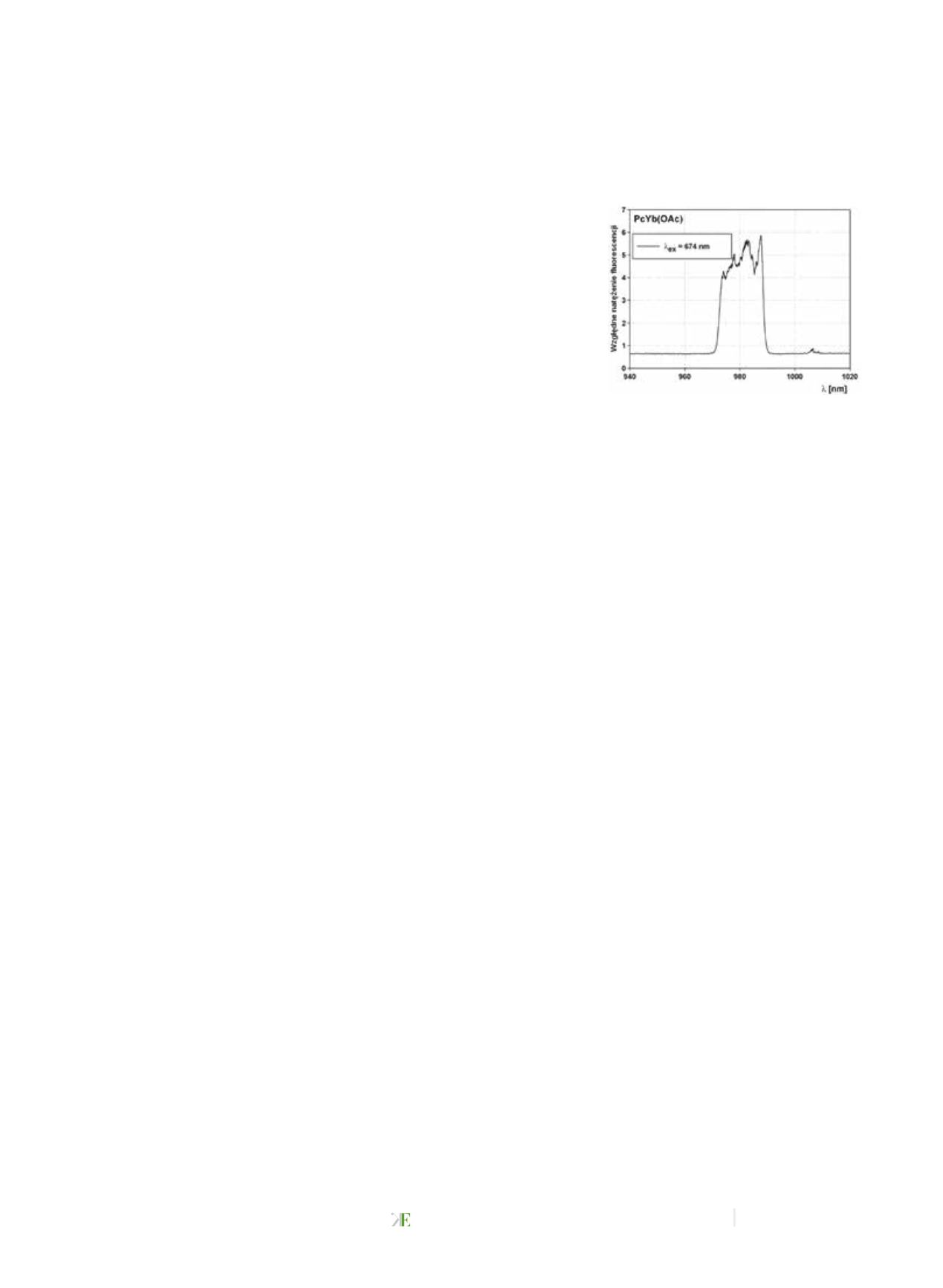
W badaniach przydatności leczniczej związków
ważna jest spektroskopowa charakterystyka połączeń
Yb(III) oraz Pr(III) [1, 12]. Ze względu na emisję Yb(III)
w podczerwieni ten zakres spektralny jest szczególnie
przydatny w terapii nowotworów (rys. 4).
Dotychczasowe badania dają nadzieję, że otrzymane
preparaty wykażą taki poziom aktywności biologicznej,
który pozwoli, po przeprowadzeniu testów klinicznych
na Uniwersytecie Medycznym we Wrocławiu, na wy-
korzystywanie ich do diagnostyki i terapii chorób no-
wotworowych skóry.
Prowadzone obliczenia modeli molekularnych dla
tych układów umożliwią znalezienie kompleksowego
podejścia do powiązania budowy cząsteczek i agrega-
tów z ich właściwościami fizykochemicznymi, głów-
nie spektroskopowymi, a w konsekwencji zależności
potencjalnej aktywności biologicznej od parametrów
optycznych układu.
Zaawansowane obliczenia modelowania moleku-
larnego DFT (
Density Functional Theory)
umożliwiły
zaproponowanie struktury molekularnej chelatów
ftalocyjaninowych Yb(III). Wygenerowane na ich pod-
stawie właściwości spektralne korelują się z wynikami
eksperymentalnymi, potwierdzając poprawność obli-
czeń [11, 12].
|
|
Wnioski
Wykorzystując możliwości che-
micznej modyfikacji porfiryn
i ftalocyjanin, można otrzy-
mywać ich pochodne o bardzo
różnorodnych właściwościach,
przydatnych w dermatologii
i kosmetyce. Prowadzone ba-
dania pozwoliły na uzyskanie
materiałów, które mogą mieć perspektywę ich efek-
tywnego wykorzystania w terapii fotodynamicznej
nowotworów.
|
|
Literatura
1.
R. Bonnett:
Porphyrins and Related Compounds: A Revised Nomencla-
ture
,
[in:] D. Dolphin (Eds.):
The Porphyrins
, Academic Press, 1, New
York 1978, 9-13.
2.
J. Sokolnicki, R. Wiglusz, S. Radzki, A. Graczyk, J. Legendziewicz:
Spectroscopic behavior of hybrid materials obtained by the sol-gel techni-
que,
Optical Mat., 26, 2004, 199-206.
3.
R.M. Ion:
Photochemical production and quenching of singlet oxygen by
the porphyrins used in PDT
,
Romanian J. Biophys., 6, 1996, 205-212.
4.
G.N. Reeke, J.W. Becker, B.A. Cunningaham, G.R. Gumther, J.L. Wang,
G.M. Endelman:
Relationships between the structure and activities of
concanavalin A
,.
Ann. N.Y. Acad. Sci., 234, 1974, 369-382.
5.
L. Brancaleon, H. Moseley:
Effects of photoproducts on the binding pro-
perties of protoporphyrin IX to protein
,
Biophys. Chem., 96, 2002, 77-87.
6.
N. Datta-Gupta, D. Malakar, J. Dozier:
Binding studies of 4 free base
porphyrins and 6 iron (+3) porphyrins with human-serum albumin
,
Rese-
arch Communications in Chemical Pathology and Pharmacology,
63,
1989, 289-292.
7.
M. Goel, D. Jain, K.J. Kaur, R. Kenoth, B.G. Maiya, M.J. Swamy, D.M.
Salunke:
Functional equality in the absence of structural similarity; an
added dimension to molecular mimicry
,
J. Biol. Chem., 276, 2001, 39277-
-39281.
8.
S.M. Andrade, S.M.B. Costa:
Spectroscopic studies on the interaction of
a water soluble porphyrin and two drug carrier proteins
,
Biophys. J., 82,
2002, 1607-1619.
9.
D.J. Toffoli, L. Gomes, N.D. Vieira Jr, L.C. Courrol:
Photodynamic poten-
tiality of hypocrellin B and its lanthanide complexes
,
J. Opt. A: Pure Appl.
Opt., 10, 2008, 104026-104034.
10.
M. Pędziwiatr, R. Wiglusz, A. Graczyk, J. Legendziewicz:
Photophy-
sics of the porphyrins and hybrid materials obtained on their basis: A pro-
spective chiral biosensor Alloys Compds
,
451,2008,46-51
11.
Y. Gerasymchuk, L. Tomachynski, I. Tretyakova, J. Hanuza, J. Legen-
dziewicz:
Axially substituted ytterbium(III) monophthalocyanine – Syn-
thesisand theirspectralproperties insolidstate,solutionand inmonolithic
silica blocks
,
J. Photochem. Photobiol. A: Chemistry, 214, 2010, 128-134.
12.
J. Legendziewicz, Yu. S. Gerasymchuk, A. Koll, J. Jański:
Photophysical
studies and application of computer modelling and Hartree-Fock method
for interpretation of spectroscopic properties and structural changes
of axially substituted Yb(III) mono-phthalocyanines in different media
,
J. Photochem Photobiol (w druku ).
Rys. 4
Widma emisji
ftalocyjaniny Yb(III) w żelu,
w zakresie podczerwieni [12]


